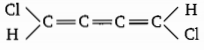The is a planar molecule where as is pyramidal because:
1. bond is more polar than bond.
2. Boron atom is bigger than nitrogen atom.
3. Nitrogen is more electronegative than boron.
4. has no lone pair but has a lone pair of electrons.
एक समतलीय अणु है जबकि पिरामिडी है क्योंकि:
1. बंध, बंध की तुलना में अधिक ध्रुवीय है।
2. बोरान परमाणु नाइट्रोजन परमाणु से बड़ा है।
3. नाइट्रोजन बोरान की तुलना में अधिक विद्युतऋणात्मक है।
4. कोई एकाकी युग्म नहीं है लेकिन इलेक्ट्रॉनों की एक एकाकी युग्म है।
Choose the correct option for the following molecule :
1. non planar
2.
3. both (1) and (2)
4.
निम्नलिखित अणु के लिए सही विकल्प चुनिए:
1. असमतलीय
2.
3. दोनों (1) और (2)
4.
What is the shape of the molecule?
1. Trigonal planar
2. Trigonal pyramid
3. T-shaped
4. Tetrahedral
अणु की आकृति क्या है?
1. त्रिकोणीय समतलीय
2. त्रिकोणीय पिरामिडी
3. T-आकृति
4. चतुष्फलकीय
According to VSEPR theory in, which species do all the atoms lie in the same plane?
1. 2.
1. 1 only
2. 2 only
3. both 1 and 2
4. neither 1 nor 2
VSEPR सिद्धांत के अनुसार, किस स्पीशीज के सभी परमाणु एक ही तल में होते हैं?
1. 2.
1. केवल 1
2. केवल 2
3. 1 और 2 दोनों
4. न तो 1 और न ही 2
Assertion : Ether behave as bases in the presence of mineral acids.
Reason : It is due to the presence of lone pairs of electrons on the oxygen atom.
अभिकथन: ईथर खनिज अम्ल की उपस्थिति में क्षार के रूप में व्यवहार करता है।
कारण: यह ऑक्सीजन परमाणु पर इलेक्ट्रॉनों के एकाकी युग्म की उपस्थिति के कारण है।
- If both the assertion and the reason are true and the reason is a correct explanation of the assertion
- If both the assertion and reason are true but the reason is not a correct explanation of the assertion
- If the assertion is true but the reason is false
- If both the assertion and reason are false
Which of the following compound does not exhibit Hydrogen bonding ?
1.
2.
3.
4.
निम्नलिखित में से कौन सा यौगिक हाइड्रोजन बंधन प्रदर्शित नहीं करता है?
1.
2.
3.
4.
The hybridisations of atomic orbitals of nitrogen in and are
1. sp, sp3 and sp2
2. sp2, sp3 and sp
3. sp, sp2 and sp3
4. sp2, sp and sp3
और में नाइट्रोजन की परमाणु कक्षाओं के संकरण हैं-
1. sp, sp3 और sp2
2. sp2, sp3 और sp
3. sp, sp2 और sp3
4. sp2, sp और sp3
The total number of -bond electrons in the following structure is
1. 4
2. 8
3. 12
4. 16
निम्नलिखित संरचना में -बंध इलेक्ट्रॉनों की कुल संख्या है-
1. 4
2. 8
3. 12
4. 16
Which of the following compound is planar and non-polar?
1.
2.
3.
4.
निम्नलिखित में से कौन सा यौगिक समतलीय और अध्रुवीय है?
1.
2.
3.
4.
Assertion : 
Reason : The molecule is slight bent T-shaped and there is repulsion between lone pairs of electrons.
अभिकथन: 
कारण : अणु थोड़ा बंकित T-आकृति का है और इलेक्ट्रॉनों के एकाकी युग्मों के मध्य प्रतिकर्षण है।
- If both the assertion and the reason are true and the reason is a correct explanation of the assertion
- If both the assertion and reason are true but the reason is not a correct explanation of the assertion
- If the assertion is true but the reason is false
- If both the assertion and reason are false