The pressure-volume plot for an ideal gas at a given temperature has the form of a
(1) Straight line
(2) Exponential curve
(3) Rectangular hyperbola
(4) U-shaped curve
एक दिए गए तापमान पर एक आदर्श गैस के लिए दाब-आयतन का आरेख है
(1) सीधी रेखा
(2) घातांकीय वक्र
(3) आयताकार अतिपरवलय
(4) U-आकार का वक्र
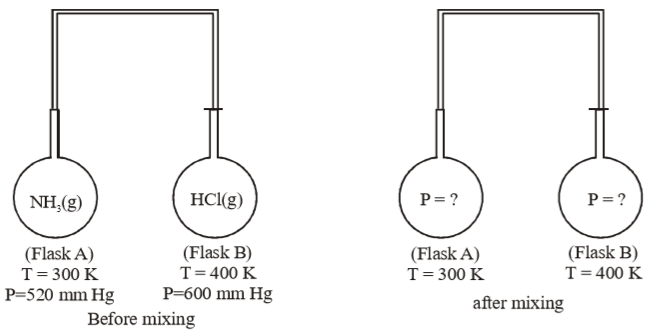
Two flasks A and B of equal volume containing and HCl gases, are connected by a narrow tube of negligible volume. The two gases were prevented from mixing by stopper fitted in connecting tube. For further detail of experiment refer to the given figure. What will be final pressure in each flask when passage connecting two tubes are opened. Assume ideal gas behaviour of and gas and the reaction.
(1) 40 mm Hg
(2) 60 mm Hg
(3) 20 mm Hg
(4) 10 mm Hg
समान आयतन वाले दो फ्लास्क A और B म और HCl गैसें होती है, जो नगण्य आयतन की एक संकीर्ण ट्यूब द्वारा जुड़ी हुई हैं। दो गैसों को जुडी हुई ट्यूब में लगे डाट द्वारा मिलाने से रोका गया। प्रयोग के और विवरण के लिए दिए गए चित्र को दिखिए। प्रत्येक फ्लास्क में अंतिम दाब क्या होगा जब दो नलिकाओं को जोड़ने वाला मार्ग खोला जाता है। और गैस का आदर्श गैस व्यवहार और अभिक्रिया को मान लीजिए।
(1) 40 mm Hg
(2) 60 mm Hg
(3) 20 mm Hg
(4) 10 mm Hg
Two vessels of capacities 3 litres and 4 litres are separately filled with a gas. The pressures are respectively 202 kPa and 101 kPa. The two vessels are connected. The gas pressure will be now, at constant temperature.
(1) 151.5 kPa
(2) 144 kPa
(3) 303 kPa
(4) 175 kPa
3 L और 4 L क्षमता के दो बर्तन अलग से एक गैस से भरे हैं। दाब क्रमशः 202 kPa और 101 kPa हैं। दोनों पात्र जुड़े हुए हैं। स्थिर तापमान पर अब गैस का दाब होगा।
(1) 151.5 kPa
(2) 144 kPa
(3) 303 kPa
(4) 175 kPa
The mean free path () of a gas sample is given by:
1.
2.
3.
4. none of these
एक गैस नमूने का माध्य मुक्त पथ () किसके द्वारा दिया जाता है:
(1)
(2)
(3)
(4) इनमें से कोई नहीं
Select the correct statement. In the gas equation PV = nRT
1. n is the number of molecules of a gas
2. V denotes the volume of 1 mole of the gas
3. n moles of the gas have a volume V
4. p is the pressure of the gas when only one mole of the gas is present
सही कथन का चयन कीजिए। PV = nRT गैस समीकरण में
(1) n गैस के अणुओं की संख्या है
(2) V, गैस के 1 मोल के आयतन को दर्शाता है
(3) गैस के n मोलों में आयतन V होता है
(4) p गैस का दाब है जब गैस का केवल एक मोल उपस्थित होता है
The correct value of the gas constant 'R' is close to
1. 0.082 L atm K
2. 0.082 L atm K-1 mol-1
3. 0.082 L atm-1 K mol-1
4. 0.082 L-1 atm-1 K mol
गैस स्थिरांक 'R' का सही मान किसके करीब है
(1) 0.082 L atm K
(2) 0.082 L atm K-1 mol-1
(3) 0.082 L atm-1 K mol-1
(4) 0.082 L-1 atm-1 K mol
The pressure in bulb dropped from 2000 to 1500 mm Hg in 47 mins. when the present in the bulb leaked through a small hole. The bulb was then completely evacuated. A mixture of and another gas of molecular weight of 79 in the molar ratio 1 : 1 at a total pressure of 4000 mm Hg was introduced. Find the mole ratio of two gases remaining in the bulb after a period of 74 mins.
(A) 1 : 1.236
(B) 1 : 2.136
(C) 1 : 3.336
(D) 2 : 1.136
बल्ब में दाब 47 min में 2000 से 1500 mm Hg तक गिर गया। जब बल्ब में उपस्थित का एक छोटे छिद्र के माध्यम से रिसाव हुआ। तो बल्ब पूरी तरह से खाली हो गया। 4000 mm Hg के कुल दाब में और अणु भार 79 वाली एक अन्य गैस के मिश्रण को 1:1 मोलर अनुपात में भरा गया। 74 min की अवधि के बाद बल्ब में बची हुई दोनों गैसों का मोल अनुपात ज्ञात कीजिए।
(1) 1 : 1.236
(2) 1 : 2.136
(3) 1: 3.336
(4) 2: 1.136
By what factor does the average velocity of a gaseous molecule increase when the
temperature (in Kelvin) is doubled?
1. 2.8
2. 4.0
3. 1.4
4. 2.0
तापमान (केल्विन में) दोगुना होने पर गैसीय अणु के औसत वेग को किस कारक से बढ़ाया जाता है?
(1) 2.8
(2) 4.0
(3) 1.4
(4) 2.0
All the three states H2O, i.e., the triple point for H2O the equilibrium,
Ice WaterVapour exist at:
1. 3.85 mm and 0.0981 C
2. 4.58 mm and 0.0098 C
3. 760 mm and 0C
4. none of the above
तीनों अवस्थाओं में H2O,अर्थात, H2O के लिए त्रिक बिंदु साम्यावस्था, बर्फजल वाष्प मौजूद है:
(1) 3.85 mm और 0.0981C
(2) 4.58 mm और 0.0098C
(3) 760 mm और 0C
(4) उपरोक्त में से कोई नहीं
Two flasks of equal volume connected by a narrow tube (of negligible volume) at 27ºC and contain 0.70 mole of at 0.5 atm. One of the flasks is then immersed into a hot bath, kept at 127ºC, while the other remains at 27ºC. Calculate the final pressure.
1. 5.714 atm
2. 0.5714 atm
3. 2.5214 atm
4. 5.5114 atm
27ºC पर एक संकीर्ण ट्यूब (नगण्य आयतन से) से समान आयतन के दो फ्लास्क जुड़े है और 0.5 atm पर 0.70 मोल होते हैं। फ्लास्क में से एक को तप्त ऊष्मक में डुबोया जाता है, 127ºC पर रखा जाता है, जबकि दूसरा 27ºC पर रहता है। अंतिम दाब की गणना कीजिए।
(1) 5.714 atm
(2) 0.5714 atm
(3) 2.5214 atm
(4) 5.5114 atm