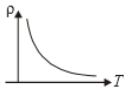
The variation of density (p) of gas with its absolute temperature (T) at constant pressure is best represented by the graph
1. 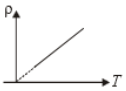 2.
2. 
3. 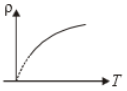 4.
4. 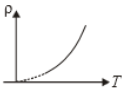
नियत दाब पर परम ताप (T) के सापेक्ष गैस के घनत्व (p) का परिवर्तन किस आरेख द्वारा सबसे अच्छी तरह से दर्शाया जाता है
1. 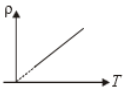 2.
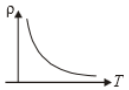
2.
3. 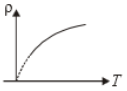 4.
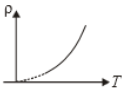
4.
 2.
2. 
 4.
4. 
 2.
2.
 4.
4.
A closed hollow insulated cylinder is filled with gas at 0°C and also contains an insulated piston of negligible weight and negligible thickness at the middle point. The gas on one side of the piston is heated to 100°C. If the piston moves 5 cm, the length of the hollow cylinder is -
(1) 13.65 cm
(2) 27.3 cm
(3) 38.6 cm
(4) 64.6 cm
एक बंद खोखले ऊष्मारोधी बेलन में 0°C ताप पर एक गैस भरी हुई है और इसके मध्य बिंदु पर नगण्य भार और नगण्य मोटाई का एक ऊष्मारोधी पिस्टन रखा गया है। पिस्टन के एक तरफ की गैस को 100° C ताप तक गर्म किया जाता है। यदि पिस्टन 5 cm से विस्थापित होता है, खोखले बेलन की लंबाई है -
(1) 13.65 cm
(2) 27.3 cm
(3) 38.6 cm
(4) 64.6 cm
Carnot cycle (reversible) of a gas represented by a Pressure-Volume curve is shown in the diagram . Consider the following statements
I. Area ABCD = Work done on the gas
II. Area ABCD = Net heat absorbed
III. Change in the internal energy in cycle = 0
Which of these are correct ?
(1) I only
(2) II only
(3) II and III
(4) I, II and III
एक गैस के कार्नो चक्र (उत्क्रमणीय) को दाब-आयतन वक्र द्वारा आरेख में दर्शाया गया है। निम्नलिखित कथनों पर विचार कीजिए
I. क्षेत्रफल ABCD = गैस पर किया गया कार्य
II. क्षेत्रफल ABCD= परिणामी अवशोषित ऊष्मा
III. चक्र में आंतरिक ऊर्जा में परिवर्तन = 0
इनमें से कौन सही हैं?
(1) केवल I
(2) केवल II
(3) II और III
(4) I, II और III
In a thermodynamic process, pressure of a fixed mass of a gas is changed in such a manner that the gas molecules absorb 30 J of heat and 10 J of work is done by the gas. If the initial internal energy of the gas was 40 J, then the final internal energy will be -
(1) 30 J
(2) 20 J
(3) 60 J
(4) 40 J
एक ऊष्मागतिकीय प्रक्रिया में, गैस के एक निश्चित द्रव्यमान का दाब इस तरह से परिवर्तित किया जाता है कि गैस के अणु 30 J ऊष्मा को अवशोषित कर लेते हैं और गैस द्वारा 10 J कार्य किया जाता है। यदि गैस की प्रारंभिक आंतरिक ऊर्जा 40 J थी, तब अंतिम आंतरिक ऊर्जा होगी -
(1) 30 J
(2) 20 J
(3) 60 J
(4) 40 J
When heat in given to a gas in an isobaric process, then
(1) The work is done by the gas
(2) Internal energy of the gas increases
(3) Both (1) and (2)
(4) None from (1) and (2)
एक समदाबीय प्रक्रम में जब गैस को ऊष्मा दी जाती है, तब
(1) गैस द्वारा कार्य किया जाता है
(2) गैस की आंतरिक ऊर्जा बढ़ती है
(3) दोनों (1) और (2)
(4) (1) और (2) से कोई नहीं
The temperature of reservoir of Carnot's engine operating with an efficiency of 70% is 1000K. The temperature of its sink is -
(1) 300 K
(2) 400 K
(3) 500 K
(4) 700 K
70% दक्षता वाले कार्नो इंजन के स्रोत का तापमान 1000K है। इसके अभिगम का तापमान है -
(1) 300 K
(2) 400 K
(3) 500 K
(4) 700 K
First law thermodynamics states that
(1) System can do work
(2) System has temperature
(3) System has pressure
(4) Heat is a form of energy
ऊष्मागतिकी के पहले नियम के अनुसार
(1) निकाय कार्य कर सकता है
(2) निकाय का तापमान होता है
(3) निकाय में दाब होता है
(4) ऊष्मा ऊर्जा का एक रूप है
The latent heat of vaporisation of water is 2240 J/gm. If the work done in the process of expansion of 1 g is 168 J, then increase in internal energy is
(1) 2408 J
(2) 2240 J
(3) 2072 J
(4) 1904 J
जल के वाष्पन की गुप्त ऊष्मा 2240 J/gm है। यदि 1g के प्रसार की प्रक्रिया में किया गया कार्य 168 J है, तो आंतरिक ऊर्जा में वृद्धि है
(1) 2408J
(2) 2240J
(3) 2072J
(4) 1904J
An ideal gas is expanded adiabatically at an initial temperature of 300 K so that its volume is doubled. The final temperature of the hydrogen gas is (γ = 1.40) [Given : ]
(1) 227.36 K
(2) 500.30 K
(3) 454.76 K
(4) –47°C
एक आदर्श गैस को 300K के प्रारंभिक तापमान पर रुद्धोष्म ढंग से प्रसारित किया जाता है ताकि इसका आयतन दोगुना हो जाए। हाइड्रोजन गैस का अंतिम तापमान है (γ= 1.40) [दिया गया है: =1.3 ]
(1) 227.36K
(2) 500.30K
(3) 454.76K
(4) –47°C
Which is the correct statement ?
(1) For an isothermal change PV = constant
(2) In an isothermal process the change in internal energy must be equal to the work done
(3) For an adiabatic change , where γ is the ratio of specific heats
(4) In an adiabatic process work done must be equal to the heat entering the system
सही कथन कौन सा है?
(1) एक समतापीय परिवर्तन के लिए PV=नियतांक
(2) एक समतापीय प्रक्रिया में आंतरिक ऊर्जा में परिवर्तन किए गए कार्य के बराबर होना चाहिए
(3) एक रुद्धोष्म परिवर्तन के लिए , जहां γ विशिष्ट ऊष्माओं का अनुपात है
(4) एक रुद्धोष्म प्रक्रिया में किया गया कार्य निकाय में प्रवेश करने वाली ऊष्मा के बराबर होना चाहिए





